 Résumé
de la conférence "Formuler la
couleur dans le verre" donnée
à Sars Poterie
Résumé
de la conférence "Formuler la
couleur dans le verre" donnée
à Sars Poterie
lors
des 6 ème
"Journées de la
Perles de Verre", 14 Septembre 2013 (révision du texte: 2016)
- par Laurent Dapolito -
1/ Ce que nous apprécions dans le verre
2/ Rappel des constituants du verre
3/ Les oxydes colorants les plus utilisés dans le verre
4/ Analyse de verres de couleur
5/ Notions de science
6/
Notre vision des couleurs, et ses limites.
7/ Le verre à l'or ou à l'argent
8/ Le verre à l'uranium
9/ L'effet "dichroïque"
1/ Pourquoi apprécions-nous cette matière,
particulièrement dans les créations artistiques ?
- Parcequ'il
peut être transpant, opaléscent
ou translucide
-
Pour sa
solidité, sa dureté, sa
longévité (il est
relativement inaltérable aux attaques chimiques)
- Sa
plasticité de mise en oeuvre, assez accessible pour le
travail au chalumeau
-
C'est une
matière noble = non poluante, recyclable, qui est
fabriquée avec des matériaux non toxiques la
plupart du temps.
Toutefois il faut tempérer: certains fabricants
font des
verres contenant des métaux lourds qui sont
à
boycotter, comme le "cristal"*, ou des verres à colorants
métaliques toxiques (chrome, cadnium, cobalt,...) ou des
aditifs
pas vraiment bio (baryum, antimoine, arsenic,...)
[*
Le "cristal" c'est à dire le verre au plomb (contenant
plus de 24 % de PbO) est un verre "basse température" qui
se stabilise assez mal, car il relargue une dose mesurable de plomb
dans les aliments lorsqu'il est utilisé dans les arts de la
table.
Sous le lobbie de la "tradition" française, la
réglementation tolère un seuil de contamination
"acceptable",
un peu comme avec l'amiante jadis. Ce verre, historiquement
réputé
pour son affinage efficace (=belle transparence), est totalement
obsolète aujourd'hui. En effet, à l'observation
visuelle: le
cristal ne peut plus être différencié
du verre ordinaire. Alors
quel est l'intérêt? N'achetez rien qui soit en
"cristal",
ce n'est pas du tout écologique]

Vitrifiant:La
silice (l'oxyde de silicium) est l'élément
principal du verre commun (autour de 70%), tel que le verre à
vitre ou verre à boire. Toutefois on peut faire des verres
"spéciaux"
ou "expérimentaux" avec d'autres
éléments. Ceux-ci
peuvent être appelé "verre" du moment qu'ils
puissent
être translucides ou transparents, avec une structure
moléculaire
amorphe ("amorphe" est le contraire de cristallisé)
Fondant:
un
verre sans fondant existe, exemple: le verre de silice pur
(appelé
abusivement "quartz"). Mais par conséquent sa
température
de fusion est très (trop) élevée (il
ne se ramolli pas en dessous
de 1300°C). Les fondants sont des oxyde alcalins qui
s'intercale
entre les molécule de silice, et qui "assouplissent" les
liaisons chimiques, abaissant le point de fusion.
Stabilisant:
Dés que l'on a mis un fondant, le verre devient sensible aux
attaques chimiques les plus simples. Donc on rajoute un produit qui
renforcera sa stabilité chimique. Un verre sans stabilisant
est un
verre qui se décomposera,
et même qui peut se dissoudre
totalement dans l'eau. Exemple: la solution de silicate de calcium
était anciennement appelé "verre soluble" (ou
"liqueur
de cailloux"), (utilisée comme colle réfractaire
par exemple).
Affinant:
Lors de sa fabrication (de la fusion de tous ses constituants) le
verre doit subir un brassage efficace pour être
homogène. Cela se
fait principalement grâce à l'ajout de
matériaux se vaporisant
dans le bain de fusion (= bullage), et une température
maximum de
liquéfaction (1400°C dans les four à
bassin). Mais cette forte
température rend le matériaux chimiquement
très réactif; il faut
maitriser le degré d'oxydation de certains constituants, on
ajoute
donc des additifs pour doser l'équilibre
d'oxydoréduction.
3/
Les
oxydes à effet colorant dans le verre les plus
utilisés : Exemples de teintes lorsqu'ils sont
utilisés seul (sans mélange):
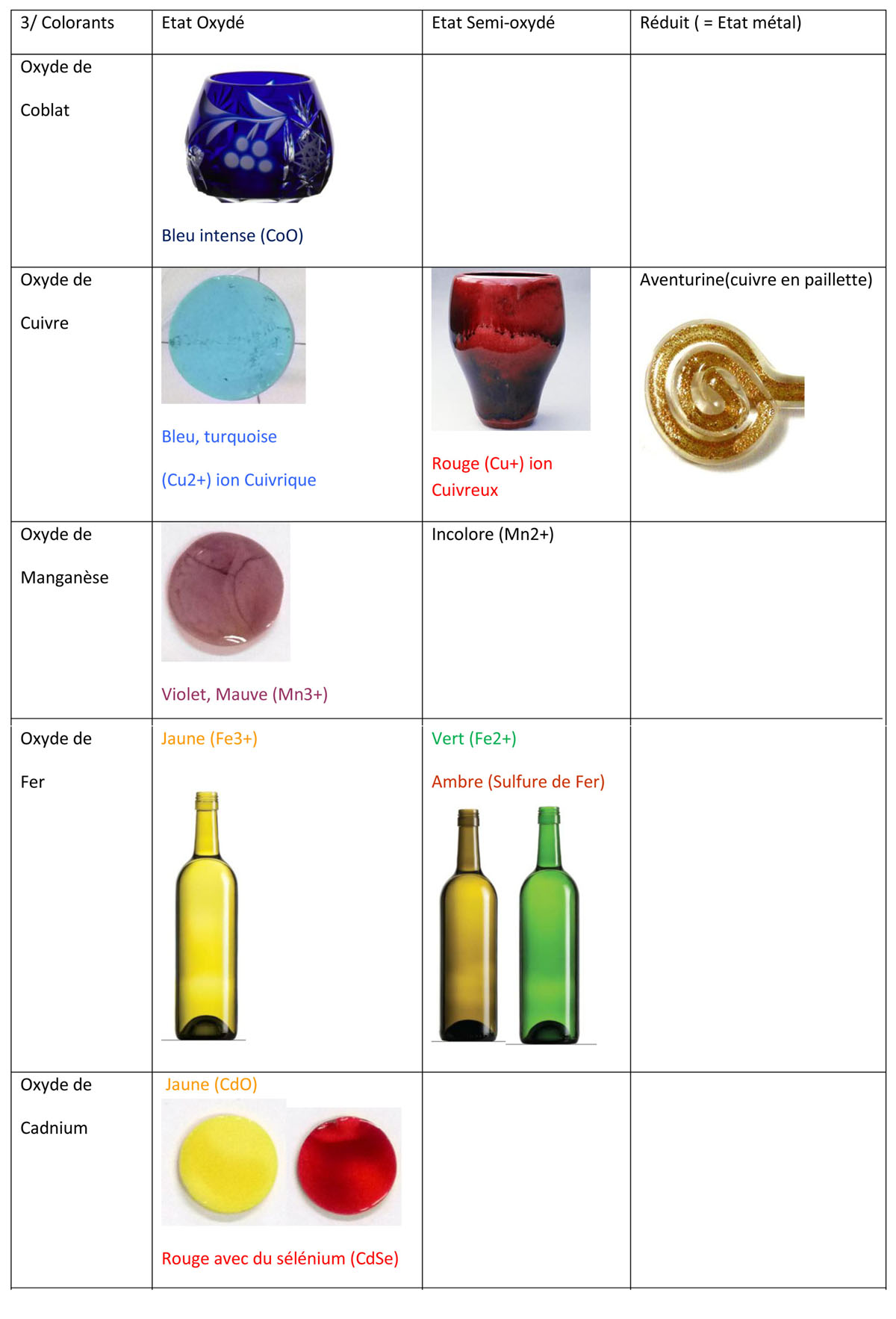

Anecdote:
l'émail des potiers est également du verre. La
coloration des
émaux se calcule de la même façon que
pour le verre, mais plus
fortement (à cause de la faible épaisseur de
l'émail). Toutefois
il y a deux contraintes supplémentaires: la possible
réaction avec
le matériaux support (donc le tesson céramique),
c'est à dire
réaction chimique et chromatique, ainsi que la
compatibilité avec
celui-ci (adhérence, tension de surface,
coefficient de
dilatation,...)
4/ Analyse comparative de verres Effetre,
2013
Echantillons
issus de baguettes
pour travail à la flamme du fabricant Effetre et leur mise
à l'analyse
par
Spectrométrie de fluorescence X (irradiation + analyse de la
rétroactionn lumineuse).
Egalement, ajout du transparent incolore très limpide du fabricant Reichenbach, pour comparaison.
Résultats: verres transparents

PS: la cas du Rubino oro : taux d'or
non
détecté (trop faible pour la machine), les
valeurs d'or
précisées ici sont la fourchette de concentration
réputée utilisée.
Résultats : verres opaques

Comparaison : Transparent / Opaque

- Commentaires des résultats d'analysse non retranscrits ici.
5/
Notions de science (interaction lumière /
matière):
Un
photon (la
lumière) arrivant sur du verre peut être :
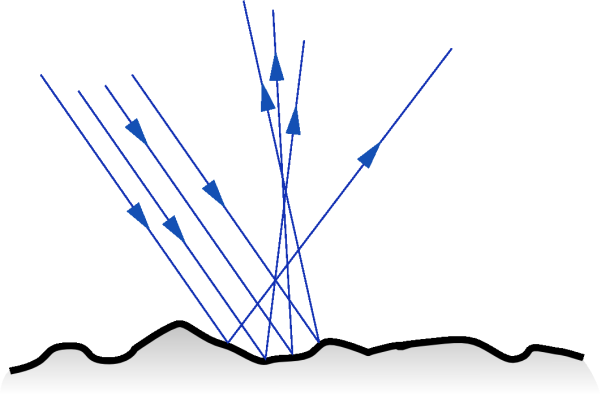
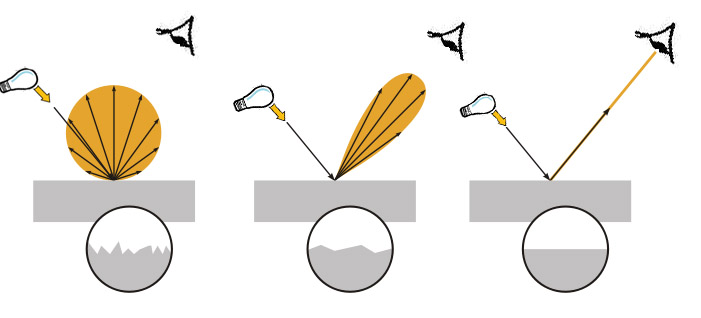
Réfléchi
de
manière diffuse (d'où une couleurs
renvoyées, d'aspect mate), ou
de manière spéculaire (effet de brillance,
éclat, et/ou effet
miroir.
Absorbé
(la
couleurs de ce photon est soustraites à la vue. Exemple: les
feuilles d'arbre sont vertes car elles absorbent le rouge et le bleu,
mais réfléchissent le vert).
Transmis
et réfracté
(donc sur verre transparent, la réfraction est la cause de
l’effet
loupe sur forme concave, par exemple).
Transmis
et dispersé
(effet de prisme ou d'arc-en-ciel : décomposition de la
lumière.
C'est utilisé par les pampilles taillées des
lustres par exemple)
Transmis
et diffusé
(effet opalescent, translucide: le photo est perturbé dans
sa
trajectoire à travers le verre)
Diffracté
(=
interférence d'ondes, mais c'est hors sujet ici et/ou trop
technique
à aborder)
Toute
la richesse de
cette diversité d'effets participe à notre
affinité pour cette
matière.


Le
photon
est une particule sans masse qui propage une vibration
électromagnétique. Cette vibration reste de
même valeur tout le
long du parcours. Donc un photon du spectre lumineux ne peut pas
changer de couleur au cours de son parcours.
Vibration
lente =
photon de faible énergie (exemple : couleur rouge,
infrarouge,
onde radio).
Vibration
rapide =
photon de haute énergie (exemple: couleur bleu, ultra
violet, rayon
X, rayon gamma)
Longueur
d’onde =
longueur parcourue par le photon en 1 oscillation
(électromagnétique). Unité :
le mètre et plus commodément
le nanomètre (nm) dans notre cas.
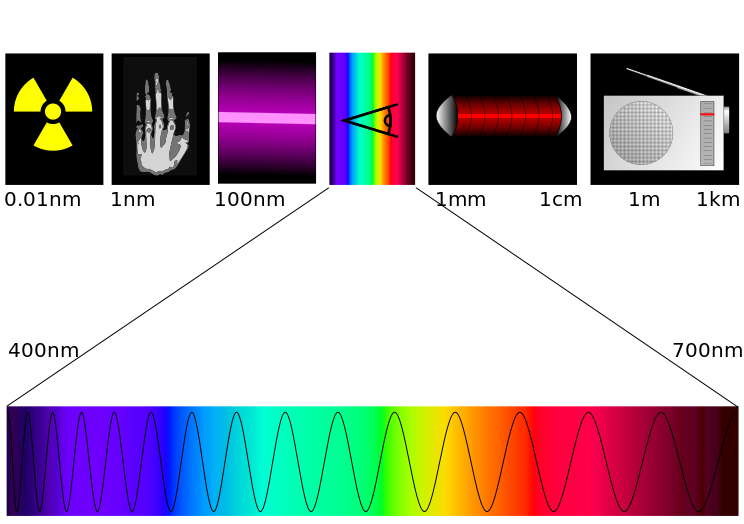
L’œil
humain est
sensible à des photons de 400nm (distinguée comme
étant bleu) à
800nm (distingué comme étant rouge).
Les
photons peuvent
réagir avec les nuages électroniques des atomes
(mais pas avec leur
noyau), et plus particulièrement (dans le cas de la
lumière) avec
les électrons des couches supérieures (les
orbitales les plus
extérieures).
En
arrivant sur un
nuage électronique, le photon peut être
absorbé: alors il transmet
son énergie à un électron.
L'électron saute vers une orbitale
plus élevé qui est stable. Cette
énergie acquise sera dissipée
progressivement par émission de photons infra rouge
(chaleur), et
l'électron retombera à son orbitale d'origine, ou
bien cette
énergie sera transmise par voisinage d’atome, Mais
si l’électron
ne trouve pas d’orbitale stable avec
l’énergie donnée par ce
photon, alors l’électron retombe
immédiatement à son état
initial en émettant un photon identique
(= de même longueur d’onde (couleur) que le photon
arrivant, et
parfois même direction) ; ainsi, dans ce cas, le photon (=
la couleur)
est renvoyée (cas du verre opaque) et/ou transmise (cas du
verre
transparent), et nous pouvons la voir.
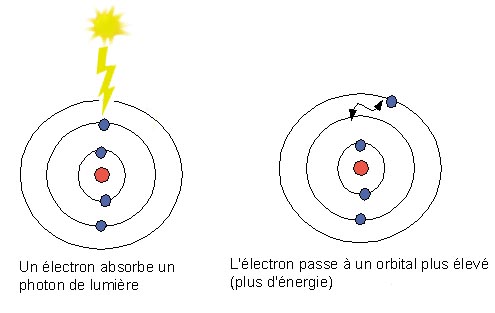
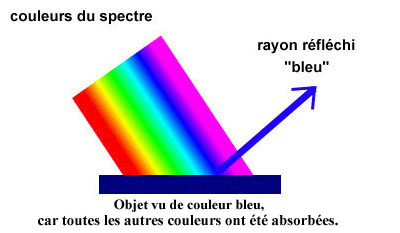
La
couleur d'un
objet est donc le résultat de l'interaction de la
lumière avec sa
matière. Au fait, quelle matière ?
Ci-dessous,
rappel
des principaux éléments entrant dans la
composition du verre,
repérés dans le tableau de Mendeleïev
(j'ai effacé les autres
éléments). Allez, un petit effort de souvenir de
vos cours de
classe du lycée.

6/
Notre vision des couleurs et ses limites.
Si
l’œil humain est
effectivement sensible à des photons de 400 à 800
nm, il ne
peut toutefois envoyer
que 3 signals au cerveau= rouge et/ou vert et/ou bleu. Et ce,
grâce à 3 sortes
de « cônes »
récepteurs (presque tous situés sur la
Fovéa de l’œil, (voir image de gauche
ci-dessous))
. Par conséquent le cerveau invente arbitrairement les
autres couleurs. Et oui !
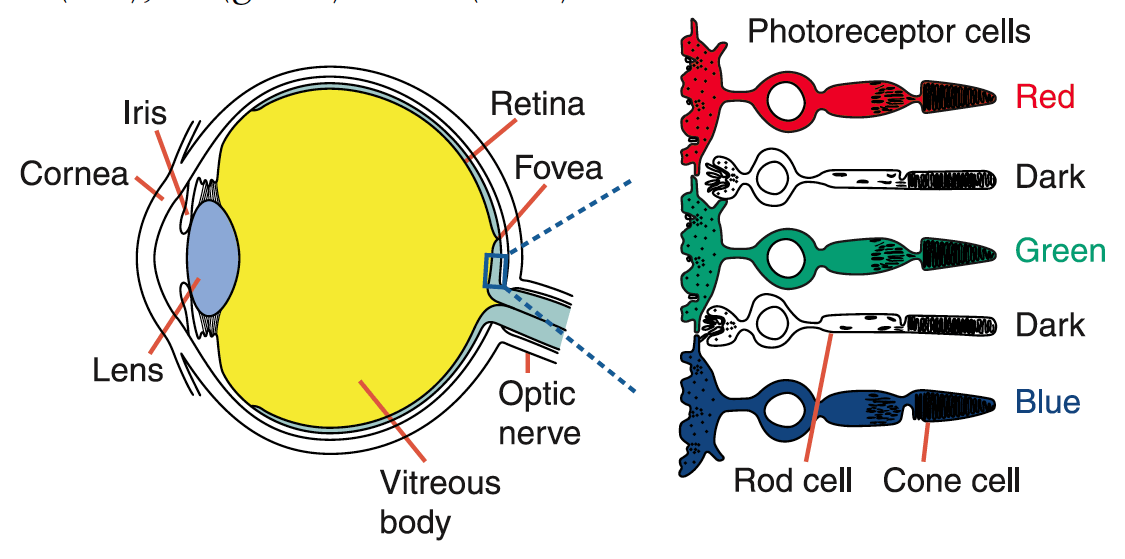




Image ci-dessus au milieu: voici un graphique
simplifié de la force du signal nerveux que l'œil
envoie au cerveau (valeurs verticales), pour chacun des
photorécepteurs (bleus, rouges et verts), en fonction de la
fréquence du photon reçu (valeurs horizontales)
Image ci-dessus à droite: les trois couleurs
primaire, et la couleurs que le cerveau voit ou imagine si on les
mélanges.
Ainsi, nous ne distinguons pas de différence entre un objet
qui émet du vrai jaune (= des photons de 590nm) et un objet
qui émet du rouge (680 nm) + vert (510 nm)
mélangé.
Démonstration : votre écran
d’ordinateur n’émet pas de photons
jaunes mais à la place : des pixels rouges + des pixels
verts (et aussi des bleus mais très peu
éclairé dans ce cas) . L'image de droite est un
zoom de votre écran, large de 3 milimètres
à l'origine. Par calcul et interprétation des
signaux nerveux de l'œil, votre cerveau invente le jaune.
Autre exemple: la lumière blanche:
l'œil humain peut croire que la lumière d'un
néon est blanc comme le soleil , malgré
qu'il lui manque beaucoup de couleurs dans son spectre lumineux. (voir
image de gauche)
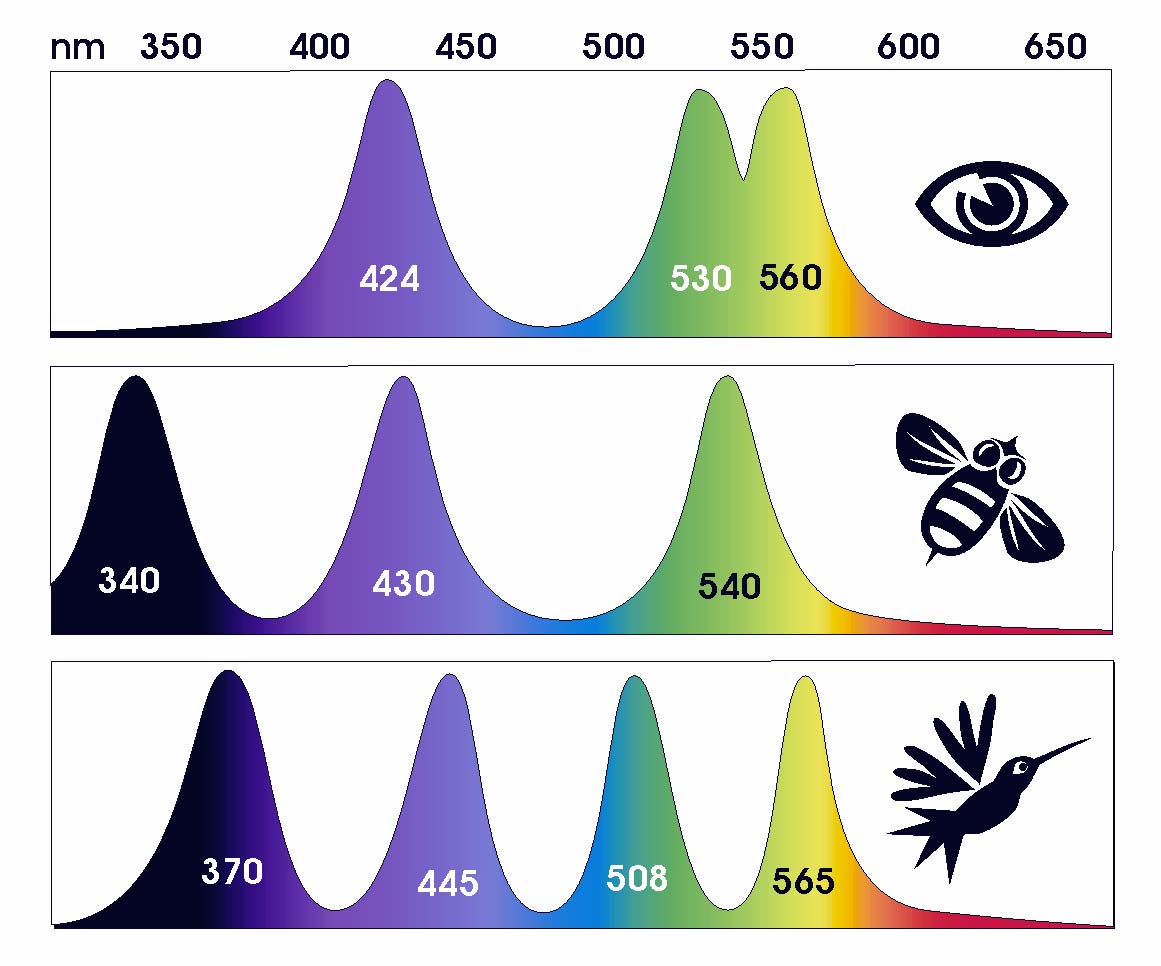
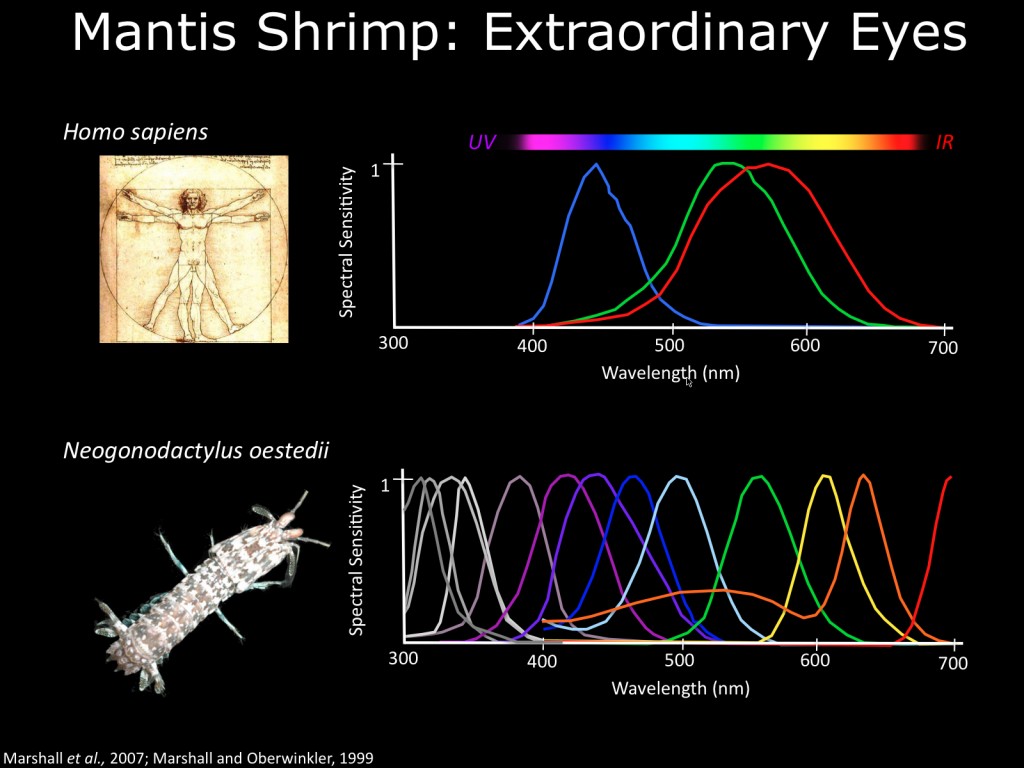
Certains animaux sont capables de discerner plus de couleurs
"primaires" que nous humains, ou bien sont
capables de voir également dans l'infrarouge (comme des
serpents) ou l'ultra-violet (comme l'abeille ou certains
oiseaux), car ils possèdent des cônes récepteurs
différents. Le stomatopode (la crevette mante), possède 12 types de cônes (elle voit donc avec 12 couleurs primaires), en plus d'avoir
6 yeux qui détecte de l’infrarouge
à l’ultraviolet ainsi que la polarité
de la lumière. Cet animal distinguerait parfaitement le
jaune, du mélange rouge + vert, que les humains voient
identiques parceque nous sommes plus limité dans nos
capaticé.

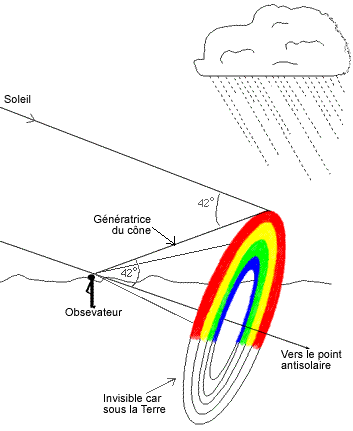
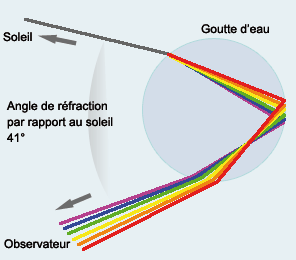
Anecdote:
Un arc en ciel est la décomposition du spectre solaire
visible (dans des gouttelettes d'eau). Chaque couleur qui en est issue
est une longueur d’onde précise et ne sont pas
mélangées. C'est pour cela que nous n'y
voyons pas toutes les couleurs. Pour discerner tous les
teintes possibles (donc avec des mélanges de
couleurs), on se repère en utilisant un diagramme
de chromaticité (triangulaire rouge-vert-bleu). Ce diagramme
(image du bas) permet aussi d'attribuer une coordonnée
graphique/informatique à une couleur.

 En
peinture, l’artiste mélange les teintes
(système soustractif des couleurs
complémentaires). Mais dans le domaine du verre, le
mélange des couleurs peut provoquer des réactions
chimiques. Un exemple bien connu est le mélange du
verre ivoire avec du turquoise: une réaction
immédiate fait noircir ces verres à leur jonction
(image de droite). On suspecte que c'est le souffre contenu
dans l'un (l'ivoire) qui est incompatible avec la recette de
l'autre verre. C’est un exemple de difficulté que
les fabricants de verre doivent surmonter pour étendre les
palettes de couleurs.
En
peinture, l’artiste mélange les teintes
(système soustractif des couleurs
complémentaires). Mais dans le domaine du verre, le
mélange des couleurs peut provoquer des réactions
chimiques. Un exemple bien connu est le mélange du
verre ivoire avec du turquoise: une réaction
immédiate fait noircir ces verres à leur jonction
(image de droite). On suspecte que c'est le souffre contenu
dans l'un (l'ivoire) qui est incompatible avec la recette de
l'autre verre. C’est un exemple de difficulté que
les fabricants de verre doivent surmonter pour étendre les
palettes de couleurs.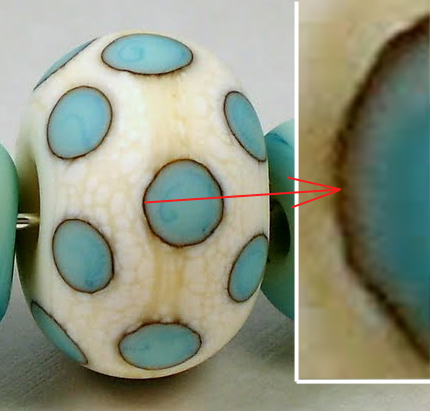
Concernant
les deux images ci-dessous,
petit rappel des couleurs primaires:
-
Vu
par un imprimeur (à droite): le papier blanc
réfléchit toute les couleurs de la
lumière naturelle blanche. Mais l'imprimeur y colle de 3
sortes d'encre, pour que le papier ne réfléchisse
plus que certaines couleur. Ainsi le papier ne renvoie que "le reste"
des couleurs de la lumière naturelle. Plus l'imprimeur
superpose de couleurs différentes, plus il supprime la
réflexion des couleurs, plus il obtient du noir.
-
Vu
par un projectionniste (à gauche, avec un
vidéoprojecteurs Tri-tubes): au début,
l'écran de cinéma est vu comme noir car il n'y a
pas de lumière dans la salle. Puis le projecteur apporte 3
couleurs. Plus le projecteur illumine chacune des couleurs au
même endroit, plus il obtient du blanc.
7/ Le verre à l'or
ou à l'argent

 Le
verre à l’or. Appelé aussi Cranberry
glass chez les anglo-saxons, Pourpre de Cassius en France, ou Rubino
oro pour le verre Italien Cette coloration est due
à des agrégats d’atomes d’or
sphériques, de taille nanoscopique (5 à
60 nm, soit un diamètre d'une longueur de 150
atomes en moyenne). Ils apparaissent vers 600 à
700°C si cette température est maintenue
suffisamment pour que les ions d’or
s’agglomèrent en bougeant très
légèrement pour réorganiser leur
liaison électronique avec leurs semblables uniquement.
Chacun de ces agrégats d’or acquiert une masse
d’électrons libres et solidaires (comme pour tout
métal conducteur
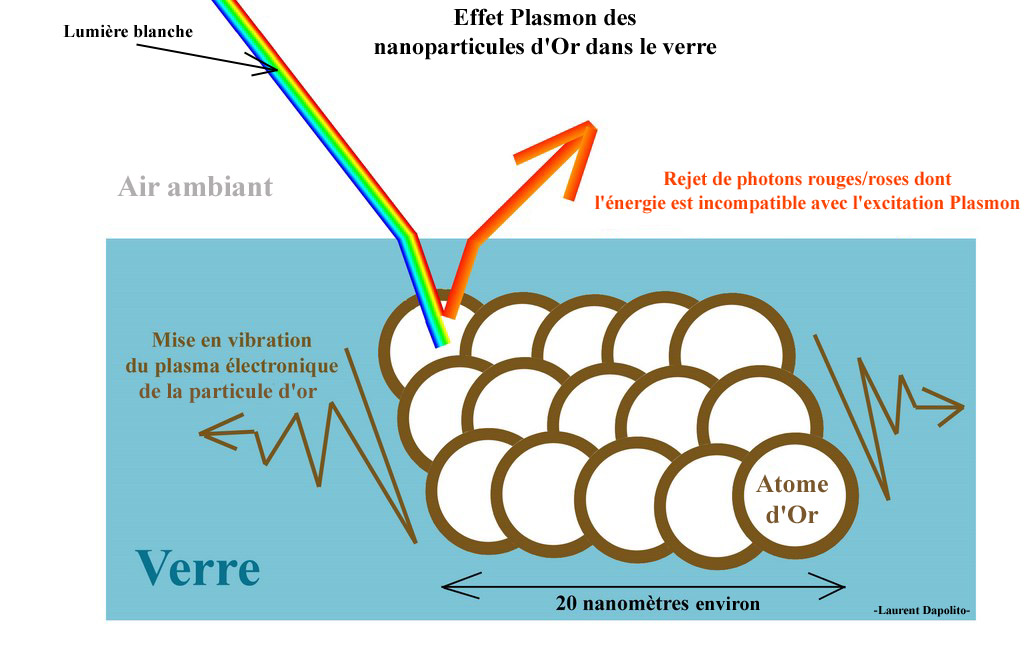
d’électricité). Lorsqu’un
photon arrive sur un atome d'or: il est absorbé
s’il peut exciter (faire vibrer) tous les
électrons libres de l'agrégat d'or. Cette mise en
vibration est possible ici grâce à la
très faible quantité
d’électrons libres solidaires, qui sont
entourés d’un isolant (ici le verre). En terme
scientifique : c’est l’effet Plasmon. Dans
notre cas, seuls les photons rouges ne véhiculent
pas l’énergie permettant ce
mécanisme ; ils sont renvoyés,
d’où la couleur observée. Si les
agrégats d’or sont trop gros (cause :
recuisson à la flamme trop longue, ou dosage d’or
initial trop fort dans le verre), alors la masse
d’électrons libres est trop lourde et sa mise en
vibration devient impossible ; la jolie couleur rouge-rose
disparaît alors.
Le
verre à l’or. Appelé aussi Cranberry
glass chez les anglo-saxons, Pourpre de Cassius en France, ou Rubino
oro pour le verre Italien Cette coloration est due
à des agrégats d’atomes d’or
sphériques, de taille nanoscopique (5 à
60 nm, soit un diamètre d'une longueur de 150
atomes en moyenne). Ils apparaissent vers 600 à
700°C si cette température est maintenue
suffisamment pour que les ions d’or
s’agglomèrent en bougeant très
légèrement pour réorganiser leur
liaison électronique avec leurs semblables uniquement.
Chacun de ces agrégats d’or acquiert une masse
d’électrons libres et solidaires (comme pour tout
métal conducteur
d’électricité). Lorsqu’un
photon arrive sur un atome d'or: il est absorbé
s’il peut exciter (faire vibrer) tous les
électrons libres de l'agrégat d'or. Cette mise en
vibration est possible ici grâce à la
très faible quantité
d’électrons libres solidaires, qui sont
entourés d’un isolant (ici le verre). En terme
scientifique : c’est l’effet Plasmon. Dans
notre cas, seuls les photons rouges ne véhiculent
pas l’énergie permettant ce
mécanisme ; ils sont renvoyés,
d’où la couleur observée. Si les
agrégats d’or sont trop gros (cause :
recuisson à la flamme trop longue, ou dosage d’or
initial trop fort dans le verre), alors la masse
d’électrons libres est trop lourde et sa mise en
vibration devient impossible ; la jolie couleur rouge-rose
disparaît alors.
Pour ce phénomène, la concentration
d’or dans le verre doit être comprise entre 0,005%
et 0,07% (en masse) , 20 à 300 ppm. Ce qui, en effet, est
très peu.
 |
Le plus ancien et
célèbre exemple de réalisation en
verre à l’or est la coupe de Lycurgue (IVe
siècle après J-C, d’origine romaine),
conservée au British Museum ; (mais ce verre
contient aussi de l’argent et un peu de cuivre).
En France, il semble que c’est Bernard Perrot (verrier
italien venu s’installer à Orléans, au
17ème siècle) qui a
relancé/redécouvert cette technique du verre
pourpre à l’or.
|
 |
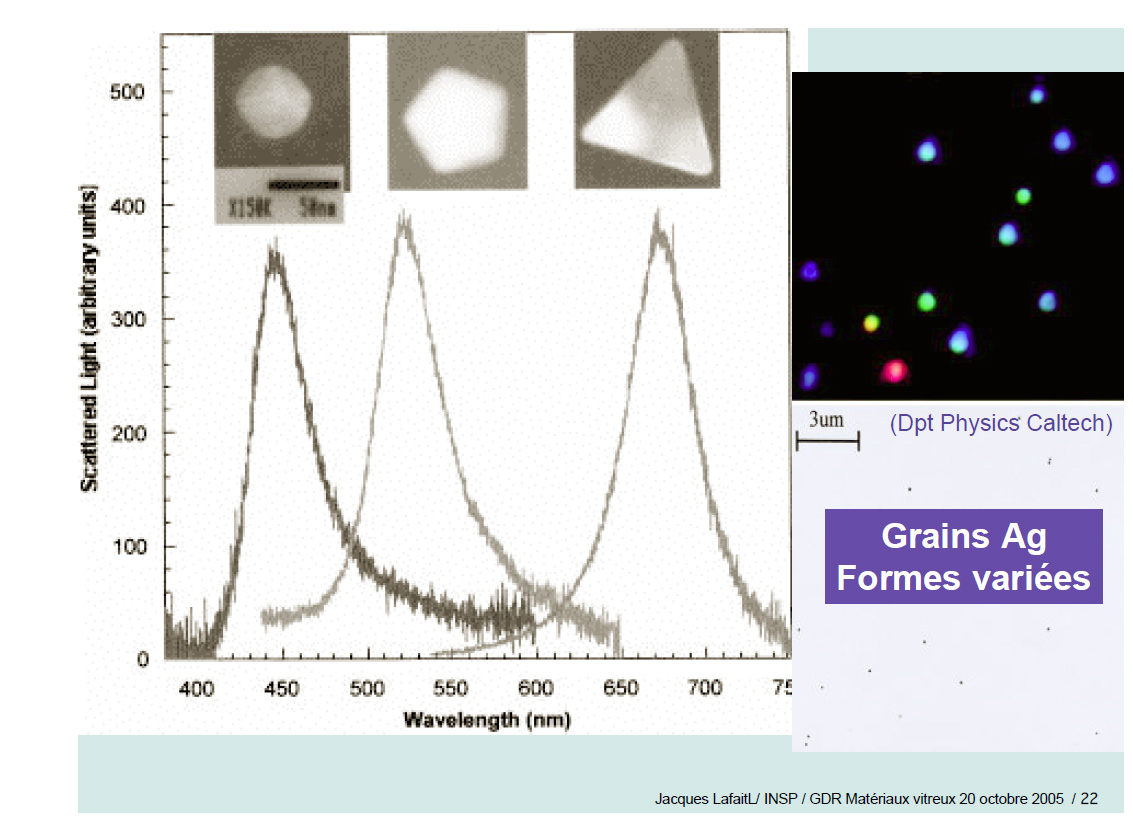
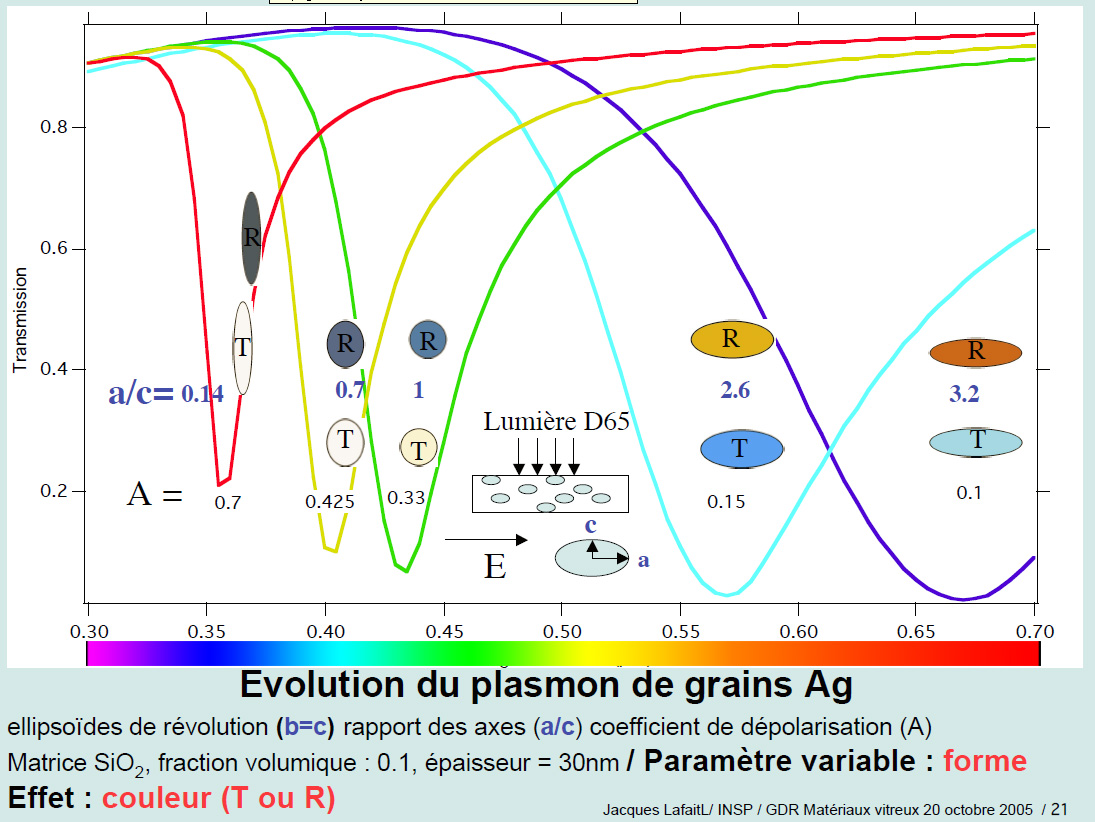
Cette
coloration par effet Plasmon fonctionne également avec
l’argent. Sauf qu’avec lui : les nanos
cristaux peuvent prendre des formes diverses en fonction de la
recuisson. Et cela permet de filtrer différentes couleurs en
fonction de ces formes. D’où parfois
l’aspect polychrome des verre à l’argent
travaillé à la flamme.


8/ Le verre à
l'uranium
 Verre
appelé aussi Vaseline glass (chez les anglo-saxons), ou
Ouraline en France. C’est un verre jaune fluorescent
contenant 0,2 à 2% d’uranium. Ce type de verre fut
produit à partir de 1830 (vaisselle décorative
essentiellement), mais il est de production assez confidentielle
aujourd’hui. Son élaboration laisse supposer un
risque de contamination pour les ouvriers et un bilan
écologique critiquable. Toutefois, le verre fini, lui, est
très peu radioactif et il reste très stable en
travail à la flamme.
Verre
appelé aussi Vaseline glass (chez les anglo-saxons), ou
Ouraline en France. C’est un verre jaune fluorescent
contenant 0,2 à 2% d’uranium. Ce type de verre fut
produit à partir de 1830 (vaisselle décorative
essentiellement), mais il est de production assez confidentielle
aujourd’hui. Son élaboration laisse supposer un
risque de contamination pour les ouvriers et un bilan
écologique critiquable. Toutefois, le verre fini, lui, est
très peu radioactif et il reste très stable en
travail à la flamme.
La fluorescence :
Dans
le cas du jaune à l’uranium : le verre se
laisse traverser par la lumière solaire blanche (=toutes les
couleurs) sauf le jaune, qu’il renvoie. Mais
à cela vient s'ajouter une deuxième
émission de photons jaunes , provenant cette fois
de l'ultraviolet, que l’atome d’uranium rejette
mais en le transformant en jaune (comme expliqué ci-dessous
*). Ainsi notre œil perçoit que l’objet
émet bien plus de jaune que ce que la lumière
visible peut normalement lui procurer. Il est
« jaune fluo ».
* Si
l’électron ne peut pas s'élever
à une orbitale stable avec
l’énergie du photon arrivant, alors
l’électron peut parfois retomber à son
état initial en deux fois. Dans ce cas, il émet
un photon de moindre énergie = d’une
autre couleur que le photon arrivant, (puis il dissipe le reste
d’énergie en infra rouge).
Et sur ce même principe, si l’électron
met longtemps à retomber à son état
initial, et donc, met longtemps à renvoyer des photons (pour
dissiper l’énergie acquise par la
lumière), alors nous assistons à un
phénomène de phosphorescence. Les verres
phosphorescents vendus aujourd'hui ne contiennent plus
d'élément radioactif.
9/ Le
verre dichroïque :
- L’effet polychrome des verres dit
« dichroïque » est
dû à une réflexion de la
lumière sur une double couche de matériau. Pour
que cet effet soit efficace, les couches (strates) d’atomes
de surface doivent être bien plans. Au niveau nanoscopique,
les ondes lumineuses arrivent sur ces deux surfaces
superposées et sont doublement
réfléchies: par la couche superficielle et celle
des profondeurs. En repartant, deux photons d’une
même couleur peuvent s’annuler s'ils vibrent en
sens opposé: cette couleur disparaît.
Par conséquent, cette couleur disparaît. Cela est
dépendant de la profondeur des strates et/ou de
l'angle de la lumière &
de l'observateur.
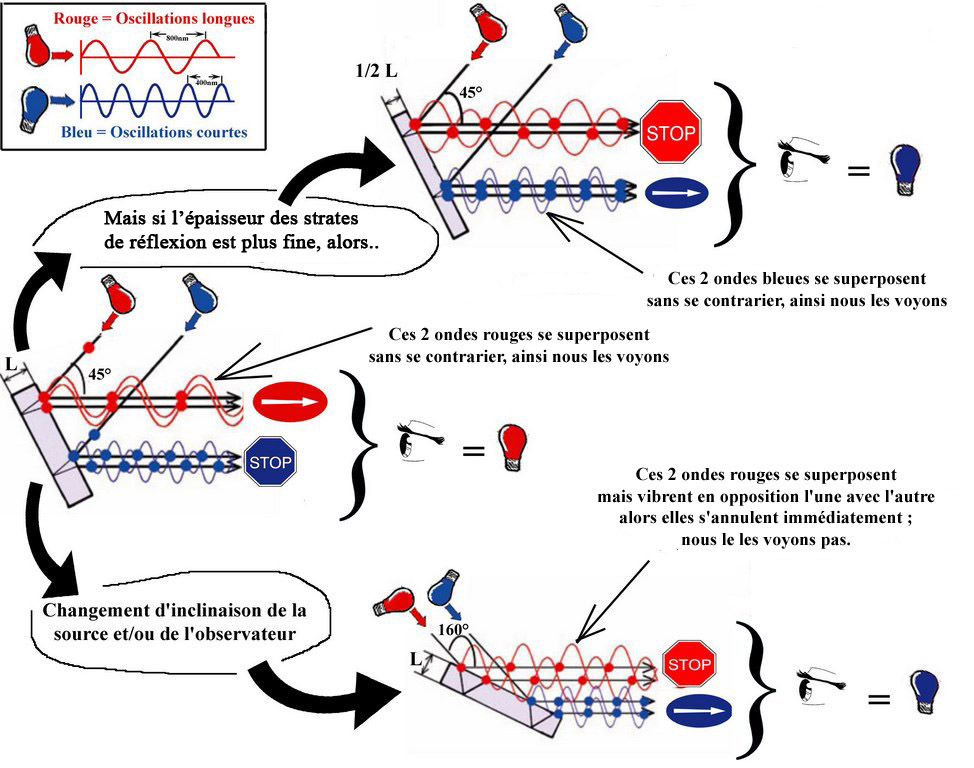
- Plus d'explication scientifique: dans le dessin ci-dessous
j’ai schématisé cet effet avec juste 2
lumières pour simplifier (rouge + bleu).
Image de gauche = état initial, puis 2 changements de
couleurs à cause de deux raisons différentes (dessins de
droites)
- Cas du dessin en haut à droite: si la
profondeur de double réflexion est plus fin, alors les photons
parcourent une distance plus courte dans le matériau. Par
conséquent, en sortie de matériau, le photon ne ressort
pas au même moment de sa vibration que dans le schéma
de gauche.
- Cas du dessin en bas
à droite: en changeant la position: en augmentant l’angle
de la source de lumière & de l’observateur : alors la
distance que le photon parcourt dans le matériau est plus
longue. Par conséquent, en sortie de matériaux, le photon
ne ressort pas au même moment de sa vibration que dans le
schéma de gauche. Ainsi dans ce schéma du bas, les photos
(vibrations) rouges réfléchies en surface et celles
réfléchies en profondeur sont exactement en
opposition : elles s’annulent, nous ne les voyons pas en
regardant l’objet. Par contre, c’est différent pour
les photons bleus. Les photons bleus réfléchis en
surface et ceux réfléchis en profondeur ne se retrouvent
pas en opposition. Nous les voyons.
C'était
le résumé de la conférence "Formuler
la couleur
dans le verre" donnée à Sars Poterie
lors des 6
ème
"Journées de la Perles de Verre", le 14 Septembre 2013 , par Laurent Dapolito











































